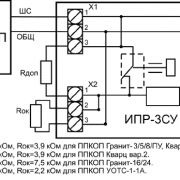
Взаимодействие углекислого газа с веществами и его химические свойства
Содержание:
- История
- Отравление угарным газом – симптомы
- Отравление угарным газом
- Применение в других сферах деятельности
- Область применения показателя
- Воздействие на организм
- Углекислый и угарный газы
- Химические свойства углекислого газа. Химические реакции (уравнения) углекислого газа:
- Ситуации, в которых «угорают»
- Четыре агрегатных состояния вещества
- [править] Литература
- Как не допустить чрезмерной концентрации угарного газа
История
Аристотель (384-322 до н.э.) впервые описал процесс сжигания углей, который приводит к образованию токсичных паров. В древности существовал способ казни – закрывать преступника в ванной комнате с тлеющими углями. Однако, на тот момент механизм смерти был непонятен. Греческий врач Гален (129-199 гг. н.э.) предположил, что имело место изменение состава воздуха, который причинял человеку вред при вдыхании. В 1776 году французский химик де Лассон произвел СО путем нагревания оксида цинка с коксом, однако ученый пришел к ошибочному выводу, что газообразный продукт был водородом, поскольку он горел синим пламенем. Газ был идентифицирован как соединение, содержащее углерод и кислород, шотландским химиком Уильямом Камберлендом Круикшанком в 1800 году. Его токсичность на собаках была тщательно исследована Клодом Бернаром около 1846 года.
Во время Второй мировой войны, газовая смесь, включающая окись углерода, использовалась для поддержания механических транспортных средств, работающих в некоторых частях мира, где было мало бензина и дизельного топлива. Внешний (с некоторыми исключениями) древесный уголь или газогенераторы газа, полученного из древесины, были установлены, и смесь атмосферного азота, окиси углерода и небольших количеств других газов, образующихся при газификации, поступала в газовый смеситель. Газовая смесь, полученная в результате этого процесса, известна как древесный газ. Окись углерода также использовалась в больших масштабах во время Холокоста в некоторых немецких нацистских лагерях смерти, наиболее явно – в газовых фургонах в Хелмно и в программе умерщвления Т4 «эвтаназия».
Отравление угарным газом – симптомы
Выраженность симптоматики зависит от концентрации вдыхаемого СО и состояния здоровья человека, главным образом, его дыхательной, нервной и сердечно-сосудистой системы.
Первые признаки отравления
- Легкая головная боль, небольшие головокружения, дискомфорт в груди;
- Слабость, сонливость, ухудшение умственной и физической активности, раздражительность;
- Повышение артериального давления;
- Тошнота, рвотные позывы.
Подобные симптомы характерны при концентрации вдыхаемого СО до 0.052% в течение 1-5 часов. При больше концентрации время на появление симптоматики снижается, а первые признаки становятся ярко-выраженными – сильные головные боли, тошнота, рвота, спутанность сознания, галлюцинации.
Основные симптомы отравления
Следующие симптомы характерны при концентрации СО до 0.094% 1-2 часов, при этом, процент соединения гемоглобина с угарным газом (карбоксигемоглобин – HbCO) составляет до 20-40%:
- Сильная головная боль, иногда пульсирующего характера, сопровождающаяся давлением в височной области;
- Головокружения, сонливость, зрительные артефакты, слезоточение, спутанность сознания, появление галлюцинаций и шумов в ушах;
- Дискомфорт и боль в груди, появление одышки, развитие тахипноэ;
- Психоэмоциональная нестабильность, страхи, ухудшение памяти, покраснение кожи;
- Тошнота, приступы рвоты;
- Нарушение координации движения, атаксия.
При тяжелом поражении появляются — обмороки, тахикардия и другие аритмии, дыхание Чейна-Стокса, конвульсии, судороги, непроизвольное мочеиспускание и дефекация, ухудшение дыхательной и сердечной функции, резкий цианоз.
Тяжелое отравление угарным газом проявляется при его вдыхаемой концентрации в 0,1-0,17 % в течение 30 минут – 2 часов. Если концентрация увеличивается до 0,5-1,2%, кома и летальный исход может наступить уже через 1-2 минуты, причем, потеря сознания происходит уже после 2-3 вдохов!
Отравление угарным газом
Окись углерода – одно из самых опасных веществ. При отравлении происходит интоксикация организма, сопровождающаяся ухудшением общего состояния человека
Очень важно вовремя распознать признаки отравления угарным газом. Результат лечения зависит от уровня вещества в организме и от того, как скоро подоспела помощь
В этом деле счет идет на минуты – пострадавший может или вылечиться окончательно, или остаться больным навсегда (все зависит от скорости реагирования спасателей).
Симптомы
В зависимости от степени отравления могут наблюдаться головные боли, головокружения, шум в ушах, учащенное сердцебиение, тошнота, одышка, мерцание в глазах, общая слабость. Часто наблюдается сонливость, что особенно опасно, когда человек находится в загазованном помещении. При попадании в органы дыхания большого количества ядовитых веществ наблюдаются судороги, потеря сознания, в особо тяжелых случаях – кома.
Первая помощь при отравлении угарным газом
Пострадавшему на месте должна быть оказана доврачебная помощь при отравлении угарным газом. Надо незамедлительно переместить его на свежий воздух и вызвать врача. Следует помнить и о своей безопасности: заходить в помещение с источником этого вещества надо только глубоко вдохнув, внутри не дышать. Пока не приехал врач надо облегчить доступ кислорода к легким: расстегнуть пуговицы, снять или ослабить одежду. Если потерпевший потерял сознание и перестал дышать, необходима искусственная вентиляция легких.
Антидот при отравлении
Специальное противоядие (антидот) при отравлении окисью углерода – это медикаментозный препарат, который активно препятствует образованию карбоксигемоглобина. Действие антидота приводит к снижению потребности организма в кислороде, поддержке органов, чувствительных к недостатку кислорода: головного мозга, печени и др. Вводится внутримышечно дозировкой 1 мл сразу после извлечения больного из зоны с высокой концентрацией ядовитых веществ. Повторно можно вводить антидот не ранее чем через час после первого введения. Допускается его использование для профилактики.
Лечение
В случае легкого воздействия окисью углерода лечение проводится амбулаторно, в тяжелых случаях больной госпитализируется. Уже в карете скорой помощи ему дается кислородная подушка или маска. В тяжелых случаях, чтобы дать организму большую дозу кислорода, пациента помещают в барокамеру. Внутримышечно вводится антидот. Уровень газа в крови постоянно контролируется. Дальнейшая реабилитация медикаментозная, действия врачей направлены на восстановление работы головного мозга, сердечно-сосудистой системы, легких.
Последствия
Воздействие угарным углеродом на организм может стать причиной серьезных заболеваний: изменяются работоспособность мозга, поведение, сознание человека, появляются необъяснимые головные боли. Особенно влиянию вредных веществ подвержена память – та часть головного мозга, которая отвечает за переход кратковременной памяти в долговременную. Последствия отравления угарным газом больной может почувствовать только спустя несколько недель. Большинство пострадавших полностью восстанавливаются после периода реабилитации, но некоторые ощущают последствия всю жизнь.
Это интересно: Стул для компьютера
Применение в других сферах деятельности
Человек также использует углекислоту в других областях деятельности и в быту. Доступность диоксида обуславливает его широкую распространенность, а свойства – востребованность даже среди обывателей.
Схема применения углекислоты
Где еще применяется углекислота:
- При сварке. Защищает металл от нагрева и окисления, обтекая электрическую дугу.
- В сельском хозяйстве. Углекислый газ в купе с солнечным светом – идеальный способ удобрить любые культуры. Распыление газа в парнике или теплице увеличивает урожайность в 2-3 раза;
- В медицине служит для создания атмосферы, близкой к реальной, при проведении искусственных операций на органах. Он применяется как стимулятор для восстановления дыхания пациента и при введении его в наркоз;
- Фармацевтика. Создает идеальную среду для синтеза химии и низкотемпературной транспортировки вод;
- Приборы и оборудование. Охлаждает оборудование и агрегаты без разбора на модули, выступает как абразивный элемент прочистки;
- Защита окружающей среды. Регулирует показатель водорода в стоках;
- Пищевая промышленность. Используется как консервант и разрыхлитель теста. Добавляется в напитки, делая их газированными;
- Для создания давления в пневматическом оружии.
Получаемый в малом количестве от спиртового брожения используется как способ газировки напитков. Он также уберегает муку, сухофрукты, арахис от насекомых, не влияя на качество и скорость их порчи.
Углекислый газ – первоклассная среда для разведения цветов, подкормки овощей и подводных растений. Он ускоряет фотосинтез и улучшает обменные процессы в растительных клетках. Главное – имеет доступную цену даже для обывателей.
Диоксид углерода может применяться и в криодеструкции, в качестве заморозки. Он сжигает холодом поверхность бородавок и родинок, заставляя их отваливаться, но не оставлять шрамов от скальпеля и швов.
Область применения показателя
Определение качества воды
Показатели содержания углерода в воде являются удобным методом определения общего качества воды. Например, некоторые страны используют анализ на ООУ (TOC) в качестве первичной проверки качества сточных и питьевых вод. Оценка содержания общего органического углерода в пробе воды – удобный аналог таких методов исследования воды, как БПК (биохимическое потребление кислорода) и ХПК (химическое потребление кислорода).
Также, существует предположение, что высокое содержание органических форм углерода в сточных водах приводит к росту биоплёнок на поверхностях трубопроводов. Это вызывает загрязнение воды, может приводить к её заражению различными патогенными и условно-патогенными микроорганизмами, что становится причиной ухудшения качества воды.
Фармацевтика и биотехнологии
Ряд фармакопей – европейская, японская, американская – считает содержание ООУ в воде ценным показателем качества воды и инструментом мониторинга биохимических процессов, происходящих в ней. Поддержание низкого уровня ООУ в питьевых водах является важным приоритетом для перечисленных стран. Считается, что существует определённое соотношение между уровнем ООУ и количеством эндотоксинов и различных микроорганизмов в воде.
Фармацевтическая промышленность, использующая биохимические процессы для производства определённых продуктов, ориентируется на этот показатель для мониторинга качества протекающих технологических процессов. Примерами использования показателя ООУ в биотехнологии можно считать производство различных биофармацевтических препаратов – вакцины, соматические клетки.
Воздействие на организм
Принцип воздействия газа на человека таков: он быстро попадает в кровь и начинает соединяться с молекулами гемоглобина; обычно они разносят кислород по организму, но в таком состоянии превращаются в карбоксигемоглобин и перестают выполнять эту ключевую для жизни функцию. Кислород оказывается запертым в крови, которая всё больше им насыщается, но в органы не попадает, из-за чего их работа останавливается и человек умирает от удушья.
Хуже всего, что поначалу это просто нельзя заметить: мало того, что у угарного газа нет запаха и он ничем себя не проявляет внешне, но и никаких неприятных ощущений от его воздействия не возникает. Когда проявляются явные симптомы, отравившийся газом чаще всего уже не в силах ничего сделать с этим сам. Тем более, что первыми приходят сонливость и вялость, а затем он просто теряет сознание.
Даже если угоревший получает помощь, возможны последствия: первым от недостатка кислорода страдать начинает мозг, так что некоторые спасённые получают его необратимые повреждения. Во многом из-за этого слово «угорелый» и его формы помимо основного значения (пострадавший от угарного газа), иногда используются и в других – например, так называют людей, ведущих себя странно и взбалмошно. Иногда последствия не проявляются сразу и отражаются на здоровье только через месяц или несколько. Возможна частичная утрата памяти, психические нарушения и другие неприятности.
К смерти приводит нахождение в течение 3 часов в помещении с концентрацией CO свыше 0,1%. Если при этом ведётся какая-то работа, отравление происходит быстрее. При повышении концентрации – гораздо быстрее. В выхлопе автомобиля CO может быть до 4-5% – именно поэтому отравиться можно не только в бане, но и в плохо проветриваемом гараже.
По тяжести выделяют три степени отравления:
- Третья, самая лёгкая. В воздухе не более 0,08% углекислого газа, а в крови до 30% карбоксигемоглобина. Отравленный ощущает боли в голове, она кружится, также может наблюдаться тошнота – иногда доходит и до рвоты. Его нужно вывести на улицу, затем дать отлежаться в хорошо проветриваемом помещении. В госпитализации нет необходимости.
- Вторая – содержание газа до 0,32%, изменённого гемоглобина в крови до 40%. Артериальное давление повышено, могут наблюдаться галлюцинации, отравленный теряет сознание. Он должен как можно быстрее оказаться на свежем воздухе, также нужна помощь медиков. На него надевают кислородную маску или защищающий от CO противогаз, подключают к кислородному баллону на несколько часов. Если помощь оказана правильно и вовремя, отравление должно обойтись без последствий.
- Первая – если карбоксигемоглобина в крови становится 50%, происходит сильное понижение давления, из-за чего возможен коллапс, слизистые сильно бледнеют, начинаются судороги, человек может впасть в кому. Последствия даже при оказании нужной помощи могут быть неблагоприятными. При особенно высокой концентрации газа смерть и вовсе наступает от одного или нескольких вдохов.
На здоровье воздействуют даже небольшие дозы, если они попадают в организм постоянно. При концентрации карбоксигемоглобина в крови до 10% явных последствий нет, но человек начинает быстро утомляться, у него плохие сон и аппетит, он становится рассеянным. Это состояние характерно для многих городских жителей, ведь из-за работы двигателей в атмосферу выбрасывается много угарного газа. Усугубляют ситуацию курильщики: при выкуривании каждой сигареты в организм также попадает немалая доза CO.
Углекислый и угарный газы
Углекислый и угарный газы:
– углекислый газ (оксид углерода(IV) – CO2) образуются при горении угля, дыхании, гниении и т.д.
– имеет кисловатый запах и вкус;
– является кислотным оксидом;
– не поддерживает горение и не горит сам, поэтому используется в огнетушителях;
– лучше растворяется в воде, чем кислород. При повышенном давлении растворимость увеличивается, что и используют при изготовлении газированных напитков. Однако, когда крышка с напитком открывается, давление становится равным атмосферному, растворимость газа снижается и жидкость словно закипает, выделяя лишний углекислый газ с характерным звуком;
– при низкой температуре и сильном давлении превращается в «сухой лед», который схож с обычным снегом и льдом. Обычно используется для перевозки мороженого;
– в лаборатории, для получения углекислого газа, используют аппарат Киппа, смешивая мрамор (CaCO3) с соляной кислотой;
– в промышленности получают при температуре в 1000 °C, разлагая известняк;
– используется для производства соды, газировки, огнетушителей и т.д.;
– так как содержание углекислого газа возрастает в составе атмосферы планеты, то молекулы газа все больше и больше задерживают тепло, не выпуская его излишки в открытый космос. Что неумолимо ведет нас всех к глобальному потеплению;
– углекислый газ накапливается в низинах, а также в закрытых помещениях, поэтому так важно проветривать закрытые помещения с большим количеством людей. Ведь даже 4% углекислого газа в воздухе хватает, чтобы возникла головная боль, участился пульс и повысилось кровяное давление;
Угарный газ
– угарный газ (оксид углерода(II) – CO) еще опаснее, так как вызывает отравление даже со смертельным исходом. Признаки отравления: головная боль, тошнота, головокружение, возможна потеря сознания. Первая помощь: вынести человека на свежий воздух, сделать искусственное дыхание;
– образуется при горении наряду с углекислым газом (при неполном сгорании угля из-за недостатка кислорода) или при взаимодействии угля и углекислого газа. При зажигании спички, синяя кайма пламени в нижней части это пламя угарного газа;
– бесцветный, без вкуса и запаха, почти нерастворим в воде;
– в противогазах есть специальный катализатор, который окисляет угарный газ до углекислого;
– угарный газ восстанавливает металлы из оксидов, как и уголь.
Химические свойства углекислого газа. Химические реакции (уравнения) углекислого газа:
Диоксид углерода относится к кислотным оксидам, поэтому для него характерны следующие химические реакции:
1. реакция взаимодействия оксида углерода (IV) и водорода:
CO2 + 4H2 → CH4 + 2H2O (t ~ 200 °C, kat = Cu2O).
В результате реакции образуются метан и вода.
2. реакция взаимодействия оксида углерода (IV) и углерода:
CO2 + C ⇄ 2CO (t = 700-1000 °C).
В результате реакции образуется оксид углерода (II). Реакция протекает при взаимодействии углекислого газа с раскаленными углями.
3. реакция взаимодействия оксида углерода (IV) и магния:
CO2 + 2Mg → 2MgO + C (t ~ 500 °C).
В результате реакции образуются оксид магния и углерод.
4. реакция взаимодействия оксида углерода (IV) и гафния:
Hf + CO2 → HfC + HfO2 (t = 800-1000 °C).
В результате реакции образуются карбид гафния и оксид гафния.
5. реакция взаимодействия оксида углерода (IV) и германия:
Ge + CO2 → GeO + CO (t = 700-900 °C).
В результате реакции образуются оксид германия и оксид углерода (II).
6. реакция взаимодействия оксида углерода (IV) и цинка:
Zn + CO2 → ZnO + CO (t = 800-950 °C).
В результате реакции образуются оксид цинка и оксид углерода (II).
7. реакция взаимодействия оксида углерода (IV) и индия:
2In + CO2 → In2O + CO (t ~ 850 °C).
В результате реакции образуются оксид индия и оксид углерода (II).
8. реакция взаимодействия оксида углерода (IV) и циркония:
2Zr + CO2 → ZrC + ZrO2 (t = 800-100 °C).
В результате реакции образуются карбид циркония и оксид циркония.
9. реакция взаимодействия оксида углерода (IV) и вольфрама:
W + 2CO2 → WO2 + 2CO (t ~ 1200 °C).
В результате реакции образуются оксид вольфрама и оксид углерода (II).
10. реакция взаимодействия оксида углерода (IV) и оксида лития:
Li2O + CO2 → Li2CO3.
В результате реакции образуется карбонат лития.
11. реакция взаимодействия оксида углерода (IV) и оксида натрия:
Na2O + CO2 → Na2CO3 (t = 450-550 °C).
В результате реакции образуется карбонат натрия.
12. реакция взаимодействия оксида углерода (IV) и оксида калия:
K2O + CO2 → K2CO3 (t ~ 400 °C).
В результате реакции образуется карбонат калия.
13. реакция взаимодействия оксида углерода (IV) и оксида бария:
BaO + CO2 → BaCO3.
В результате реакции образуется карбонат бария.
14. реакция взаимодействия оксида углерода (IV) и оксида кальция:
CaO + CO2 → CaCO3.
В результате реакции образуется карбонат кальция.
15. реакция взаимодействия карбоната кальция, оксида углерода (IV) и воды:
CaCO3 + CO2 + H2O → Ca(HCO3)2.
В результате реакции образуется гидрокарбонат кальция.
16. реакция взаимодействия оксида углерода (IV) и оксида магния:
MgO + CO2 → MgCO3.
В результате реакции образуется карбонат магния.
17. реакция взаимодействия оксида углерода (IV) и оксида кремния (II):
SiO + CO2 → SiO2 + CO (t ~ 500 °C).
В результате реакции образуются оксид кремния (IV) и оксид углерода (II).
18. реакция взаимодействия оксида углерода (IV) и воды:
CO2 + H2O ⇄ H2CO3.
В результате реакции образуется угольная кислота.
19. реакция взаимодействия оксида углерода (IV) и гидроксида лития:
2LiOH + CO2 → Li2CO3 + H2O.
В результате реакции образуются карбонат лития и вода. В ходе реакции используется концентрированный раствор гидроксида лития.
20. реакция взаимодействия оксида углерода (IV) и гидроксида калия:
KOH + CO2 → KHCO3,
2KOH + CO2 → K2CO3 + H2O.
В первом случае в результате реакции образуются гидрокарбонат калия, во втором случае – карбонат калия и вода. Реакция протекает в первом случае в этаноле и используется разбавленный раствор гидроксида калия, во втором используется концентрированный раствор гидроксида калия.
21. реакция взаимодействия оксида углерода (IV) и гидроксида натрия:
NaOH + CO2 → NaHCO3,
2NaOH + CO2 → Na2CO3 + H2O.
В первом случае в результате реакции образуются гидрокарбонат натрия, во втором – карбонат натрия и вода. В ходе первой реакции используется разбавленный раствор гидроксида натрия, в ходе второй – концентрированный раствор гидроксида натрия.
22. реакция взаимодействия оксида углерода (IV) и гидроксида кальция:
Ca(OH)2 + CO2 → CaCO3 + H2O.
В результате реакции образуются карбонат кальция и вода.
23. реакция взаимодействия оксида углерода (IV) и гидроксида бария:
Ba(OH)2 + CO2 → BaCO3 + H2O.
В результате реакции образуются карбонат бария и вода.
24. реакция взаимодействия оксида углерода (IV) и метана:
CH4 + CO2 → 2CO + 2H2 (t = 800-900 °C, kat = NiO, нанесенный на Al2O3).
В результате реакции образуются оксид углерода (II) и вода.
25. реакция термического разложения оксида углерода (IV):
2CO2 → 2CO + O2 (t > 2000 °C).
В результате реакции образуются оксид углерода (II) и кислород.
26. реакция фотосинтеза:
6CO2 + 6H2O → C6H12O6 + 6O2 (hv, kat = хлорофилл).
В результате реакции образуются глюкоза и кислород.
Ситуации, в которых «угорают»
Пожар
Человек в первую очередь задыхается от дыма. Это, конечно, не только угарный газ, но и токсические продукты сгорания всякой синтетики и пластмассы. Причем отравиться дымом могут не только жильцы пострадавшей квартиры, но и соседи сверху. Неисправные газовые приборы. Если с пожаром все понятно, то поломки в колонке непрофессионалу заметить трудно. Вроде работает как всегда, может пламя только не такое голубое, но кто на него смотрит?
Газовые приборы
Особенно опасны газовые водонагреватели в ванной комнате. Закрытое пространство, запертая дверь…10 минут, сознание теряем, а на помощь никто не придет. Основная причина – нарушение в вентиляционном дренаже и самостоятельно установленные газовые приборы. К этой категории относятся плиты, работающие на метане. Не забывайте открывать окна во время готовки!
Смерть в гараже
Уж сколько мы слышали этих ужасных историй! Молодые, полные сил, часто парами (мужчина и женщина), целыми компаниями. И ведь слышали, и знают. Но почему то опять надеемся на «авось», на то, что «я же не дурак». И заводят двигатель в гараже. В основном с целью согреться в холодное время, ведь гараж для мужчины – второй дом, там он свободу чувствует. Опять же с друзьями бухнуть можно, о бабах поговорить. Или ремонтом заняться. В выхлопных газах содержится до 3% CO, в старых карбюраторных двигателях может доходить до 10%. В закрытом гараже смерть наступает в течение 5 минут после заведения мотора. Но мало кто знает, что отравление может наступить и при открытой двери гаража, просто это займет чуть больше времени.
Печки и камины
Раньше это была самая частая причина угорания – преждевременно закрытая заслонка печной трубы. Нужно поймать момент, когда горящего огня уже нет, но угли еще красные и не остыли. Печей сейчас все меньше, но они есть. Загородные дома с каминами, бани, сауны, отапливаемы дровами. Теплые такие, натуральные, с приятным запахом. Но да, и они могут стать причиной смерти.
Приспособления для гриля и барбекю
Ну очень любит русский человек мясо. Особенно пожаренное на углях. Мужчина при этом представляет себя почти добытчиком в первобытно-общинном социуме. Но от цивилизации не уйдешь. Есть спрос – есть предложение. Вот вам переносные установки для гриля. Где хотите, там и ставьте, с собой в поход берите, на дачу, на охоту, на рыбалку. Конечно, жарить надо на улице, все знаем. А если мясо уже замариновано, а погода испортилась? Не отменять же. Перемещаемся опять таки в гараж, или в палатку. Алкоголь – наш постоянный спутник. Праздник удался. Но не всегда…
Отравление на автостраде
Вы знаете, что на оживленной дороге с интенсивным движением иногда возникает смертельная концентрация угарного газа? Человек может отравиться, если находится рядом с трассой, или в автомобиле с открытым окном. Был случай, когда дальнобойщик уснул в своей машине, припаркованной на обочине, а окно не закрыл. Да, он не проснулся. Сюда же можно отнести смерти за рулем в туннелях. Или в забуксовавшем автомобиле, когда вентиляция выхлопных газов нарушена.
Четыре агрегатных состояния вещества
Газообразное состояние вещества – одно из трех «классических». Помимо него, выделяются также твердые и жидкие вещества. В последнее время в учебниках встречается определение и четвертого агрегатного состояния – плазмы. Это ионизированные (частично или полностью) газы. Четвертый тип агрегатного состояния был выявлен при изучении космоса, и, оказывается, он встречается во Вселенной чаще всего. Плазма – это составная часть многих планет, основа звезд, туманностей, высших слоев атмосферы Земли.
Далее речь пойдет о газах. Они были открыты сравнительно недавно, позже жидких и твердых веществ, так как не поддавались изучению человеческим глазом. Развитие науки в сфере газообразных соединений началось с XVII века.
[править] Литература
- Б. В. Некрасов. Основы общей химии. — М.: «Химия», 1967, — т.2
- Я. А. Угай. Высшая и неорганическая химия. — М.: «Высш. шк.», 1997, — 527 с.
| Обычные оксиды | CO2 • CO |
|---|---|
| Экзотические оксиды | C2O2 • C2O3 • C3O2 • C4O2 • C4O6 • C5O2 • C2O • CO3 • CO4 • C12O9 • C12O12 |
| Полимеры | Оксид графита • C3O2 • CO • CO2 |
| Производные оксидов углерода | Карбонилы металлов • Угольная кислота • Гидрокарбонаты • Карбонаты • Дикарбонаты • Трикарбонаты |
| Общеядовитого действия | Циановодород (AC) • Хлорциан (CK) • Арсин (SA) • Фосфин (PH) • Угарный газ (CO) | ||||||
|---|---|---|---|---|---|---|---|
| Удушающего действия | Фосген (CG, Р-10 • Дифосген (DP) • Хлор (CL) | ||||||
| Кожно-нарывного действия | Иприт (HD) • Люизит (L, Р-43) • Метилдихлорарсин (MD) • Этилдихлорарсин (ED) • Фенилдихлорарсин (PD) • Сесквииприт (Q) • Азотистые иприты (Газ HN1, Газ HN2, Газ HN3) • Кислородный иприт (T) | ||||||
| Нервно-паралитического действия |
|
||||||
| Раздражающего действия (ирританты) |
|
||||||
| Психохимического действия (инкапаситанты) |
Хинуклидил-3-бензилат (BZ, Р-78) • Фенциклидин (SN) • ЛСД (K) • Апоморфин • EA 3167 | ||||||
| Болевого действия (алгогены) | 1-метокси-1,3,5-циклогептатриен (CH) | ||||||
| Метаболические яды (цитотоксиканты) |
1,2-дихлорэтан • Оксид этилена • Полихлордибензодиоксины (ПХДД) • Полихлордибензофураны (ПХДФ) |
Как не допустить чрезмерной концентрации угарного газа
Учитывая, какими могут быть последствия отравления, важно отнестись к своей безопасности внимательно. Что минимизировать риск, следует выполнять несколько пунктов:
- При использовании печи или газового котла для отопления проводить регулярные проверки. Специалисты должны осматривать технику как минимум раз в год.
- Если система отопления в доме собственная, вы в любом случае в группе риска: полностью проблемы не исключены даже при регулярных осмотрах и содержании техники в отличном состоянии. Поэтому следует оснастить жильё датчиками CO. При слабом превышении нормы они издают сигналы, а при сильном сигнал становится непрерывным.
- Нельзя полностью перекрывать вентиляцию даже для сохранения тепла – лучше проснуться в холодной комнате, чем рисковать не проснуться вообще.
- Если датчики установили утечку и сигнализируют о сильном превышении аварийного порога, следует сразу же покинуть помещение. Респиратор и даже оснащённый угольным фильтром противогаз обеспечивают лишь частичную защиту, так что рисковать линий раз не стоит.
- В бане нельзя находиться долго при закрытой заслонке печи и красных углях: горение продолжается и выделяется угарный газ, он не может уйти в трубу и остаётся внутри.
- Ещё один источник опасности – кальян. Если в него поступает мало кислорода, CO накапливается и можно получить лёгкое отравление. При первых признаках –тошноте или головной боли, следует немедленно прекратить пользоваться кальяном и проветрить помещение, во время проветривания лучше выйти на свежий воздух.
Интересно, что раньше в качестве своеобразных датчиков использовали канареек: даже при малом превышении стандартной концентрации угарного газа они переставали петь и падали замертво. Это очень сильно помогало шахтёрам избегать той же участи, ведь при добыче угля и металлов отравление CO – одна из главных опасностей.