Сероводород (h2s)
Содержание:
- Способы очистки воды от сероводорода
- Синтез
- Производители оборудования для получения и очистки сернистого газа
- Причины
- Физико-химические свойства
- Сероводород в природе и жизнедеятельности человека
- Сероводород, формула, молекула, строение, состав, вещество:
- Очистка
- Сероводород в естественной среде
- Природа окислительно-восстановительных реакций серы и водорода
- Немного цифр
Способы очистки воды от сероводорода

Пример напорной очистки воды, где жидкость подаётся в ёмкость через распылители
Если вы не знаете, что делать, чтобы привести свой колодец в порядок, то прислушайтесь к рекомендациям специалистов.
Чтобы удалить запах, появляющийся сразу после подачи воды в систему, нужно провести первоначальное отстаивание жидкости. В этом случае при контакте воды с кислородом сероводород просто улетучится. Однако отстаивать водичку просто дома в кастрюлях не рекомендуется. Для такого случая можно делать и использовать два вида резервуаров:
В первом случае используются большие пластиковые бочки ёмкостью 200-300 литров. В них вода подаётся через специальные распылители по типу душевой лейки, которые обеспечивают взаимодействие жидкости с кислородом. Причём резервуары должны быть открытого типа (то есть без верхней крышки). В результате газ окисляется и улетучивается. Уже из такого резервуара после очистки вода может подаваться в чистом виде в дом, если установлена хорошая насосная система.
Важно: использовать металлические бочки в этом случае нельзя, поскольку сероводород разрушает железо
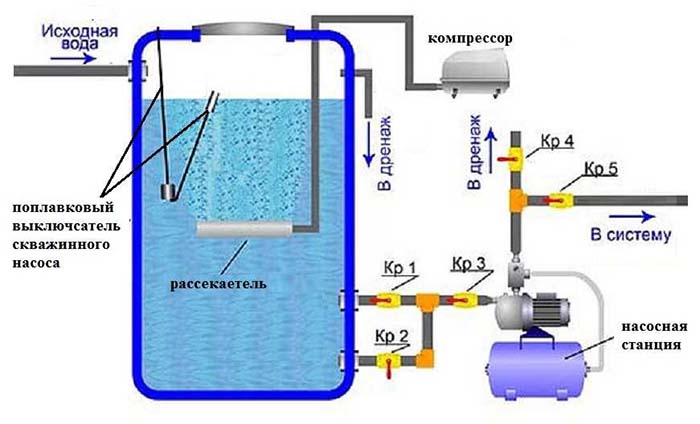
Пример аэрации воды при помощи компрессора
Напорные системы для очистки воды от сероводорода работают по другому принципу. Здесь вода из колодца проходит через фильтры и заполняет резервуар. Потом под напором жидкость поднимается к верхней части бочки и уже отправляется по системе в дом. Таким образом, происходит отстаивание воды, а газ улетучивается с её поверхности после поднятия к высшей точке. Делать тот или иной вид отстойника нужно в зависимости от ваших предпочтений и финансовых возможностей.
Очистка через окисление
Можно использовать и другую систему очистки воды от сероводорода. В этом случае используются химикаты в виде серы или гипохлорида натрия, добавляемые в воду. В результате происходит реакция сероводорода с химическими элементами и газ испаряется. Доочистить воду помогают здесь специальные фильтры с зернистым содержимым.
Важно: замена фильтра в такой системе очистки должна быть регулярной. Если пропустить этот момент, то вместе с водой вы рискуете получить вредные для здоровья химикаты
Использование сорбентов
Пример работы и устройства угольного фильтра для очистки воды от сероводорода
Еще один способ, при помощи которого можно избавиться от запаха сероводорода — это применение угольного фильтра. В его состав входит гранулированный активированный уголь, который отлично окисляет вредные соединения в воде и собирает их на себя
Важно производить замену фильтра в соответствии с рекомендациями
Замена нагревательного оборудования
Если случается так, что пахнет неприятно вода именно после нагревания, то в этом случае нужно обратить особенное внимание на нагревательную систему. Бывает, что на стенках нагревательного прибора от времени скапливаются вредные серные или нитратные бактерии, которые осуществляют свою жизнедеятельность, а при нагревании ещё и активизируются
В этом случае рекомендуется либо почистить нагревательный элемент, либо полностью заменить его.
Важно: оттягивать с удалением запаха сероводорода из воды ни в коем случае не стоит. Здоровье домочадцев — прежде всего
Синтез
Синтез сероводорода можно проводить в две стадии:
- путем смешивания серы и опилками железа обеспечивается сгоревший в Tet (производство белого и едкий сольфатаре), давая своего рода оранжевый гальки (в сульфид железа FeS) с серыми следами (опилки , которые не вступают в реакцию);
- при заливке любой кислоты (предпочтительно серной кислоты , но реагирует именно ион гидроксония ) на сульфид железа, полученный на первом этапе, немедленно происходит интенсивное выделение сульфида. водорода, легко узнаваемого по его запаху, описанному в школьных учебниках как «тошнотворное», которое вызывает тухлое яйцо.
Сульфид алюминия Al 2 S 3 также может реагироватьс водой, которая образует, помимо H 2 S, гидроксид алюминия .
Производители оборудования для получения и очистки сернистого газа
Оборудование для получения и очистки сернистого газа производит узкое число производителей. С целью закупки соответствующих установок производителям нужно обращаться в специализированные компании, которые предоставляют услуги по обустройству и реконструкции промышленных предприятий.
Среди производителей можно отметить компании:
- «Дальневосточный завод энергетического машиностроения» (Дальэнергомаш), занимающийся производством нагнетателей сернистого газа 400-12-2, 700-13-1, 1050-13-1, Э 1700-11-2М;
- Российское приборостроительное предприятие «ОПТЭК» специализируется в области аналитического приборостроения и занимается выпуском хемилюминесцентного газоанализатора диоксида серы в атмосферном воздухе.
Причины
Сероводородная вода образуется при таких условиях:
- заиливание дна и стенок труб, когда источник давно не чистился
- попадание биологических объектов внутрь
- закупоренные водоносные горизонты (характерно для глубоких скважин)
- потеря герметичности обсадной колонной, что приводит к попаданию внутрь сульфитных бактерий
- во время бурения попался пласт с сульфидными рудами
- длительные или сильные осадки, паводки, которые насыщают водоносные горизонты органикой и химическими веществами, служащими питанием для бактерий
- попадание серных соединений в процессе устройства источника
- загрязнения техногенного характера.
Физико-химические свойства
Сероводород — бесцветный газ с сильным запахом тухлых яиц. Водный раствор сероводорода бесцветный без характерного аромата.
Соединение имеет молекулярную массу 34,1 г / моль, водный раствор имеет плотность 1,334 г / мл. Он имеет температуру плавления -82 ° С и температуру кипения -60 ° С. Он слабо растворяется в воде и способен растворять всего 4 грамма на литр этого растворителя при 20 ° C (Royal Society of Chemistry, 2015).
Сероводород реагирует как кислота и как восстановитель. Он взрывается при контакте с дифторидом кислорода, пентафторидом брома, трифторидом хлора, оксидом дихлорида и фульминатом серебра. Он может воспламениться и взорваться под воздействием медного порошка в присутствии кислорода..
Он может реагировать аналогичным образом с другими порошкообразными металлами. Воспламеняется при контакте с оксидами и пероксидами металлов (пероксид бария, триоксид хрома, оксид меди, диоксид свинца, диоксид марганца, оксид никеля, оксид серебра, диоксид серебра, триоксид таллия, пероксид натрия, оксид ртути, оксид кальция).
Зажигается броматом серебра, гипохлоритом свинца (II), хроматом меди, азотной кислотой, оксидом свинца (IV) и оксидом. Он может воспламениться, если пройдет через ржавые железные трубы. Экзотермически реагирует с основаниями.
Тепло реакции с кальцинированной содой, гидроксидом натрия, гидроксидом калия, гидроксидом бария может вызвать возгорание или взрыв непрореагировавшего участка в присутствии воздуха / кислорода (HYDROGEN SULFIDE, 2016).
Сероводород в природе и жизнедеятельности человека
Сероводород входит в состав вулканических газов, природного газа и газов, сопутствующих месторождениям нефти. Много его и в природных минеральных водах, например, в Черном море он залегает на глубине от 150 метров и ниже.
Сероводород применяют:
- в медицине (лечение сероводородными ваннами и минеральными водами);
- в промышленности (получение серы, серной кислоты и сульфидов);
- в аналитической химии (для осаждения сульфидов тяжелых металлов, которые обычно нерастворимы);
- в органическом синтезе (для получения сернистых аналогов органических спиртов (меркаптанов) и тиофена (серосодержащего ароматического углеводорода).Еще одно из недавно появившихся направлений в науке — сероводородная энергетика. Всерьез изучается получение энергии из залежей сероводорода со дна Черного моря.
Сероводород, формула, молекула, строение, состав, вещество:
Сероводород (сернистый водород, сульфид водорода, дигидросульфид) – бесцветный газ со сладковатым вкусом с характерным неприятным тяжёлым запахом тухлых яиц (тухлого мяса).
Сероводород – бинарное химическое соединение водорода и серы, имеющее формулу H2S.
Химическая формула сероводорода H2S.
Строение молекулы сероводорода, структурная формула сероводорода:
Сероводород – наиболее активное из серосодержащих соединений.
Сероводород тяжелее воздуха. Его плотность составляет 1,539 кг/м3, по отношении к воздуху – 1,19. Поэтому скапливается в низких непроветриваемых местах.
@ https://www.youtube.com/watch?v=RYZkPRGcc0k
Сероводород плохо растворяется в воде. Раствор сероводорода в воде – очень слабая сероводородная кислота. Хорошо растворим в бензоле, этаноле, бромэтане, гексане, додекане, октане, толуоле, трихлорэтилен, хлорбензоле.
Термически устойчив при температурах менее 400 °C. При температурах более 400 °C разлагается на составляющие – простые вещества: водород и серу.
В отличие от воды, в сероводороде не образуются водородные связи, поэтому сероводород в обычных условиях не сжижается.
Сероводород является сверхпроводником при температуре 203 К (-70 °C) и давлении 150 ГПа.
Сероводород коррозионно активен, поэтому предъявляются дополнительные требования при разработке нефтяных, газовых и газоконденсатных месторождений, содержащий сероводород.
Чрезвычайно огнеопасен. Смеси сероводорода и воздуха взрывоопасны. Возможно возгорание на расстоянии. Горит синим пламенем.
Соли сероводородной кислоты (раствор сероводорода в воде) называют сульфидами. В воде хорошо растворимы только сульфиды щелочных металлов, аммония. Сульфиды остальных металлов практически не растворимы в воде, они выпадают в осадок в ходе химических реакций. Многие сульфиды ярко окрашены. Многие природные сульфиды в виде минералов являются ценными рудами (пирит, халькопирит, киноварь, молибденит).
Сероводород в природе встречается редко, в незначительных количествах в составе природного газа, попутного нефтяного газа, сланцевого газа, а также в вулканических газах, в растворённом виде – в нефти, сланцевой нефти и в природных водах. Например, в Чёрном море слои воды, расположенные глубже 150-200 м, содержат растворённый сероводород (концентрация 14 мл/л).
Образуется при гниении белков, которые содержат в составе серосодержащие аминокислоты метионин и (или) цистеин. Небольшое количество сероводорода содержится в кишечных газах человека и животных.
Сероводород высокотоксичен и ядовит. Предельно допустимая концентрация (ПДК) сероводорода в воздухе населенных пунктов в России – 0,008 мг/м3, в России – 0,007 мг/м3.
Порог ощутимости запаха составляет 0,012-0,03 мг/м3. При вдыхании воздуха с небольшими концентрациями у человека довольно быстро возникает адаптация к неприятному запаху «тухлых яиц» и он перестаёт ощущаться. Во рту возникает сладковатый металлический привкус. При вдыхании воздуха с большой концентрацией из-за паралича обонятельного нерва запах сероводорода почти сразу перестаёт ощущаться.
При острых отравлениях возникает жжение и боль в горле при глотании, конъюнктивит, одышка, головная боль, головокружение, слабость, рвота, тахикардия, возможны судороги. Смертельная концентрация составляет 830 мг/м3 в течение 30 минут или 1100 мг/м3 в течение 5 минут.
При высокой концентрации сероводорода однократное вдыхание может вызвать мгновенную смерть.
Очистка
Желательно провести исследование, чтобы определить причину и правильно очистить воду от сероводорода. Далее, существует несколько вариантов действий.
Обработка скважины
Стандартные методы такие:
- удаление ила и отложений на дне, трубах, элементах системы. Они содержат магний с железом, которыми питаются бактерии. Это нужно делать периодически через каждые 1,5 — 2 года
- прокачка с удалением слоя песка и глины. После этого на дно засыпается крупный гравий или щебень, служащий природным фильтром
- герметизация обсадных труб или их замена
Дегазация
Если вода пахнет сероводородом, то ее можно отстаивать в емкостях, поскольку он является летучим веществом, а при столкновении с кислородом аэробные серобактерии умирают. Но эффективнее использовать специальные аппараты — дегазаторы, так жидкость будет очищена еще в трубах на пути к точкам водозабора в доме. При этом осуществляют также подкисление.
Разновидности дегазаторов:
- безнапорный. Это большая открытая пластиковая емкость, вода поступает в него по распылительным форсункам, происходит «душирование» — насыщение кислородом. Бак вместе с компрессором, накачивающим воздух или без него, устанавливают под крышей здания, чтобы образовалась самотечная система;
- напорный. Более удобный. Имеет меньший объем, работает быстрее. Он оборудованный, кроме компрессора, специальным насосом, нагнетающим воду. Его можно ставить в любом месте, включая подвалы, цоколи.
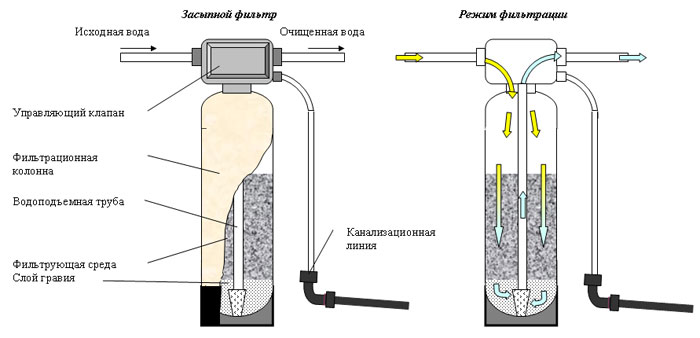
Напорная дегазационная установка
Установка и процесс аэрации напорным оборудованием:
- Обустраивается кессон или делается углубление возле насосной станции или в ином месте
- В подготовленное место помещают аэратор с компрессором и насосом
- Вода поступает в закрытый бак, в котором предусмотрен клапан для выпуска удаляемого газа
- Внутрь накачивается кислород, что помогает удалить сероводород
После кислородного окисления нужно применять катализаторы для образования нерастворимых соединений. Распространено использование таких веществ:
- активированного угля
- магнетита, графита
- марганцованного песка. Опасность марганцевых соединений в том, что появляются их соли, которые нужно удалять
- перманганата калия (образовывает коллоидную серу)
Химическая обработка
В ее процессе окисление провоцируются не кислородом, а другими вещества: перекисем водорода, озоном, гипохлоридом натрия. При этом образуется нерастворимый осадок, который останавливается фильтрами с активными реагентами. Этот метод используется также в масштабах городских трубопроводов.
Наиболее безопасным является перекись водорода, которая образует нерастворимую серу, удаляемую через угольный фильтр. Это поможет полностью избавиться от запаха. Используют также иониты для ускорения процессов окисления.
Сорбционно-каталитическое фильтрование
Очистка от сероводорода осуществляется реагентами, ускоряющими процесс окисления, собирающими и нейтрализующими вредные вещества: препаратами из активированного или каменного угля, кремния, шунгита, различными сорбентами. Они помещаются в специальные капсулы, которые крепятся на краны или трубы. Блоки с ними периодически надо менять или промывать.
Такие фильтры применяют, когда вода сероводородная и не заражена иными бактериями, а также после дезинфекции, если обнаружены патологические микроорганизмы. Кроме сорбента там должны быть окислители. Они слабо эффективные против серьезных загрязнений, поскольку предназначены только для тонкой очистки. Их используют в комплексных решениях вместе с другими аппаратами.
Водонагреватель
Иногда дурной запах появляется только после включения нагревателя. Это значит, что на поверхности ТЭНов образовались отложения, в которых размножаются сульфатрецудирующие микроорганизмы. Эти элементы необходимо тщательно промыть, а на подводящие трубы установить фильтр с сорбентом.
Обезжелезивание
Насчитывают 5 различных соединений железа, содержащихся в скважинах. Если они обнаружены, производится обезжелезивание — применяются реагенты, преобразовывающие данный элемент в осадок, который отфильтровывается. На входящие трубы устанавливают фильтры с несколькими секциями, с окислительными внутренними поверхностями и элементами, собирающими осадок.
Самыми эффективными комплексными решениями, которыми производится удаление сероводорода из воды, являются модульные очистительные системы, состоящие из аэрационных колонн, блоков окисления, сорбционных элементов для тонкой очистки.
Используют также габаритные установки с отстойниками. Тогда процедура пройдет все возможные стадии.
Сероводород в естественной среде
Микробный: цикл серы
Ил из пруда; черный цвет из-за сульфидов металлов
Сероводород является центральным участником цикла серы , биогеохимического цикла серы на Земле.
При отсутствии кислорода , серы , уменьшая и сульфатредуцирующие бактерий , получают энергию от окислительного водорода или органических молекул путем уменьшения элементарной серы или сульфата до сероводорода. Другие бактерии выделяют сероводород из серосодержащих аминокислот ; это вызывает запах тухлых яиц и способствует запаху метеоризма .
Поскольку органическое вещество разлагается в условиях с низким содержанием кислорода (или гипоксии ) (например, в болотах, эвтрофных озерах или мертвых зонах океанов), сульфатредуцирующие бактерии будут использовать сульфаты, присутствующие в воде, для окисления органического вещества, производя сероводород в виде трата. Часть сероводорода будет реагировать с ионами металлов в воде с образованием сульфидов металлов, которые не растворимы в воде. Эти сульфиды металлов, такие как сульфид железа FeS, часто имеют черный или коричневый цвет, что приводит к темному цвету шлама .
Некоторые группы бактерий могут использовать сероводород в качестве топлива, окисляя его до элементарной серы или сульфата, используя растворенный кислород, оксиды металлов (например, оксигидроксиды железа и оксиды марганца ) или нитраты в качестве акцепторов электронов.
В пурпурных серных бактериях и зеленые серные бактерии используют сероводород в качестве донора электронов в процессе фотосинтеза , в результате чего получают элементарную серу. Этот способ фотосинтеза старше, чем режим цианобактерий , водорослей и растений , который использует воду в качестве донора электронов и высвобождает кислород.
Биохимия сероводорода — ключевая часть химии мира железо-сера . В этой модели происхождения жизни на Земле геологически полученный сероводород постулируется как донор электронов, приводящий к восстановлению углекислого газа.
Животные
Сероводород смертелен для большинства животных, но некоторые узкоспециализированные виды ( экстремофилы ) действительно процветают в местах обитания, богатых этим соединением.
В глубоком море гидротермальные источники и холодные выходы с высоким уровнем сероводорода являются домом для ряда чрезвычайно специализированных форм жизни, от бактерий до рыб. Из-за отсутствия солнечного света на этих глубинах эти экосистемы полагаются на хемосинтез, а не на фотосинтез .
Пресноводные пружины богаты сероводородом, в основном , домом для беспозвоночных, но и включать в себя небольшое количество рыбы: Cyprinodon bobmilleri (а pupfish из Мексики), Limia sulphurophila (а poeciliid из Доминиканской Республики ), Gambusia eurystoma (а poeciliid из Мексики), и несколько Poecilia (поецилииды из Мексики). Беспозвоночные и микроорганизмы в некоторых пещерных системах, таких как пещера Мовиле , адаптированы к высоким уровням сероводорода.
Межзвездное и планетарное явление
Сероводород часто обнаруживается в межзвездной среде. Это также происходит в облаках планет в нашей солнечной системе.
Массовые вымирания
Цветок сероводорода (зеленый), растянувшийся на 150 км вдоль побережья Намибии. Когда бедная кислородом вода достигает побережья, бактерии в богатых органическими веществами отложениях производят сероводород, токсичный для рыб.
Сероводород был причастен к нескольким массовым вымираниям , произошедшим в прошлом Земли. В частности, накопление сероводорода в атмосфере могло вызвать или, по крайней мере, способствовало пермско-триасовому вымиранию 252 миллиона лет назад.
Органические остатки на этих границах вымирания указывают на то, что океаны были бескислородными (обедненными кислородом) и имели виды мелкого планктона, которые метаболизировали H2S . Образование H2S, возможно, был вызван массивными извержениями вулканов, в результате которых в атмосферу были выброшены углекислый газ и метан , которые нагрели океаны, снизив их способность поглощать кислород, который в противном случае окислял бы H2S . Повышенный уровень сероводорода мог привести к гибели растений, производящих кислород, а также к истощению озонового слоя, вызывая дальнейший стресс. Маленький H2Цветение S было обнаружено в наше время в Мертвом море и в Атлантическом океане у побережья Намибии .
Природа окислительно-восстановительных реакций серы и водорода
Реакция образования сероводорода является окислительно-восстановительной:
Н₂⁰ + S⁰→ H₂⁺S²⁻
Процесс взаимодействия серы с водородом легко объясняется строением их атомов. Водород занимает первое место в периодической системе, следовательно, заряд его атомного ядра равен (+1), а вокруг ядра атома кружится 1 электрон. Водород с легкостью отдает свой электрон атомам других элементов, превращаясь в положительно заряженный ион водорода — протон:
Н⁰ -1е⁻= Н⁺
Сера находится на шестнадцатой позиции в таблице Менделеева. Значит, заряд ядра ее атома равен (+16), и количество электронов в каждом атоме также 16е⁻. Расположение серы в третьем периоде говорит о том, что ее шестнадцать электронов кружатся вокруг атомного ядра, образуя 3 слоя, на последнем из которых находится 6 валентных электронов. Количество валентных электронов серы соответствует номеру группы VI, в которой она находится в периодической системе.
Итак, сера может отдать все шесть валентных электронов, как в случае образования оксида серы(VI):
2S⁰ + 3O2⁰ → 2S⁺⁶O₃⁻²
Кроме того, в результате окисления серы, 4е⁻могут быть отданы ее атомом другому элементу с образованием оксида серы(IV):
S⁰ + О2⁰ → S⁺4 O2⁻²
Сера может отдать также два электрона c образованием хлорида серы(II) :
S⁰ + Cl2⁰ → S⁺² Cl2⁻
Во всех трех вышеуказанных реакциях сера отдает электроны. Следовательно, она окисляется, но при этом выступает в роли восстановителя для атомов кислорода О и хлора Cl.
Однако в случае образования H2S окисление — удел атомов водорода, поскольку именно они теряют электроны, восстанавливая внешний энергетический уровень серы с шести электронов до восьми. В результате этого каждый атом водорода в его молекуле становится протоном:
Н2⁰-2е⁻ → 2Н⁺,
а молекула серы, наоборот, восстанавливаясь, превращается в отрицательно заряженный анион (S⁻²):
S⁰ + 2е⁻ → S⁻²
Таким образом, в химической реакции образования сероводорода окислителем выступает именно сера.
С точки зрения проявления серой различных степеней окисления, интересно и еще одно взаимодействие оксида серы(IV) и сероводорода — реакция получения свободной серы:
2H₂⁺S-²+ S⁺⁴О₂-²→ 2H₂⁺O-²+ 3S⁰
Как видно из уравнения реакции, и окислителем, и восстановителем в ней являются ионы серы. Два аниона серы (2-) отдают по два своих электрона атому серы в молекуле оксида серы(II), в результате чего все три атома серы восстанавливаются до свободной серы.
2S-² — 4е⁻→ 2S⁰ — восстановитель, окисляется;
S⁺⁴ + 4е⁻→ S⁰ — окислитель, восстанавливается.
Немного цифр
По степени воздействия на организм вредные вещества подразделяются на четыре класса опасности: 1-й – вещества чрезвычайно опасные; 2-й – вещества высокоопасные; 3-й – вещества умеренно опасные; 4-й – вещества малоопасные.
Сероводороду (H2S) — наиболее активному из серосодержащих соединений — присвоен второй класс опасности. По данным ВОЗ (Всемирной Организации Здравоохранения), он входит в перечень самых распространённых и наиболее опасных загрязнителей окружающей среды наряду с дихлорметаном, формальдегидом, стиролом, толуолом, мышьяком, окисью углерода, свинцом, фтором, ртутью т.п. Сероводород считается одним из самых нежелательных компонентов нефтепереработки.
В случае выброса предприятием этого отхода в окружающую среду может быть возбуждено дело, что наглядно продемонстрировал недавний случай с московским нефтеперерабатывающим заводом в Капотне, который подозревают в «обогащении» столичного воздуха сероводородом в количестве, превысившем ПДК (предельно допустимая концентрация) в 51(!) раз. Многочисленные жалобы населения на неприятный запах из окон, резь в глазах и привкус во рту и произведённые затем замеры воздуха не смогли оставить равнодушным даже видавший всякое Росприроднадзор.
Сероводород хорошо растворим в воде. Диапазон взрывоопасных концентраций в смеси его с воздухом достаточно широк и составляет от 4 до 45% об. При контакте с металлами (особенно если в газе содержится влага), сероводород вызывает сильную коррозию. Предельно допустимая концентрация сероводорода (H2S) в воздухе в рабочей зоне—10 мг/м3 (кубометр), в смеси с углеводородами —3 мг/м3.
Предельно допустимая норма сероводорода (H2S) в воздухе населенных мест—0,008 мг/м3 (миллиграмм на кубический метр)
Ощутимый запах сероводорода отмечается при концентрации 1,4—2,3 мг/м3, значительный запах —при 4 мг/м3, тяжелый запах при 7—11 мг/м3.
Бесцветный газ с неприятным запахом тухлых яиц, не только ядовит, но и коварен: при очень высоких концентрациях он уже после первых вдохов блокирует обонятельный нерв, и человек перестаёт чувствовать этот запах после того, как тот «ударил в нос». Острое отравление наступает уже при концентрациях 0,2–0,3 мг/л, а концентрация выше 1 мг/л — смертельна.
Смертельная концентрация этого газа в воздухе очень мала – всего 0,1%. Такое количество сероводорода может привести человека к летальному исходу за 10 минут. Стоит лишь немного увеличить концентрацию – и смерть наступает мгновенно, после первого же вдоха. Для примера: в канализационной системе концентрация сероводорода иногда достигает 16%.
Если речь идёт о незамкнутом помещении, сероводород не действует так резко и внезапно, не застаёт жителей врасплох. Однако, человеку свойственно привыкать к любому запаху, это некоторая защитная реакция нашего организма (например, жители мегаполисов не замечают специфический запах в метро, не замечают запах выхлопных газов, но при этом очень впечатляются свежестью приморского воздуха, будучи в отпуске). Именно с этим явлением сталкиваются периодически жители больших городов по всему миру, и в частности, Москвы, где в некоторых районах подобный запах – привычное дело.
Что касается промзон и градообразующих предприятий, известно, что люди, работающие или живущие в непосредственной близости от заводов с сероводородными (и иными) выбросами (в концентрациях от 0,02%), испытывают так называемое хроническое отравление. Выражается это, как правило, в стабильно плохом самочувствии, головных болях, потере веса, металлическом привкусе во рту (тревожный сигнал, посылаемый печенью), неприятными ощущениями в груди и даже обмороками, обострениях хронических заболеваний.
Поскольку экзогенный (вызываемый внешними причинами) сероводород попадает в организм через дыхательные пути, первый удар всегда принимает слизистая оболочка. Этот газ плохо действует и на глаза: может вызвать конъюнктивит, спровоцировать светобоязнь, раздражение слизистой оболочки глаз, снижение остроты зрения.